Szerkesztő:Alfa-ketosav/perklorát
From Wikipedia, the free encyclopedia
A perklorát perklorátiont (ClO−4), a perklórsav konjugált bázisát tartalmazó vegyület (só). A kation lehet fémion, kvaterner ammóniumion vagy más ion, például NO+2.
| Alfa-ketosav/perklorát | |||
 A perklorát váza kötéshosszokkal és -szögekkel | |||
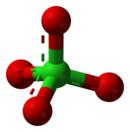 A perklorát pálcikamodellje |  A perklorát kalottamodellje | ||
| Szabályos név | Perklorát[1] | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 14797-73-0 | ||
| PubChem | 123351 | ||
| ChemSpider | 109953 | ||
| DrugBank | DB03138 | ||
| MeSH | 180053 | ||
| ChEBI | 49706 | ||
| |||
| InChIKey | VLTRZXGMWDSKGL-UHFFFAOYSA-M | ||
| Gmelin | 2136 | ||
| UNII | VLA4NZX2P4 | ||
| ChEMBL | 1161634 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | ClO4 | ||
| Moláris tömeg | 99,45 g/mol | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A perklorát jelenthet ezenkívül perklórsavésztereket (kovalens perklorát).[2] Ezek a perklórsav alkil- vagy arilészterei. Itt az oxigén és a szerves csoport kötése kovalens.
A legtöbb ionos perklorátban a kation gyengén koordinál. Számos sót pirotechnikai eszközökben használnak oxidánsként és élelmiszer-csomagolásban a statikus elektromosság irányítására.[3] Ezenkívül használják rakéta-hajtóanyagként, trágyaként és a papír- és textiliparban fehérítőként.
Az étel és a víz perklorátszennyezése az egészségre káros és elsősorban a pajzsmirigyet érinti.
Az ionos perklorátok általában színtelen, vízoldékony szilárd anyagok. A perklorátion a vízben való oldódáskor a keletkezik a disszociáció során. Sok perklorát oldódik a vízen kívül más oldószerben is.[4] 4 perkloráttartalmú vegyület van forgalomban, az NH4ClO4, a HClO4, a KClO4 és a NaClO4.