
Amoníaco
compuesto químico / De Wikipedia, la enciclopedia encyclopedia
Estimado Wikiwand AI, Seamos breves simplemente respondiendo estas preguntas clave:
¿Puede enumerar los principales datos y estadísticas sobre Amoníaco?
Resumir este artículo para un niño de 10 años
El amoníaco, amoniaco,[5][6] azano, espíritu de Hartshorn, trihidruro de nitrógeno o gas de amonio es un compuesto químico de nitrógeno con la fórmula química NH3. Es un gas incoloro con un característico olor repulsivo. El amoníaco contribuye significativamente a las necesidades nutricionales de los organismos terrestres por ser un precursor de fertilizantes. Directa o indirectamente, el amoníaco es también un elemento importante para la síntesis de muchos fármacos y es usado en diversos productos comerciales, sirve para la elaboración de cosméticos y tintura de cabello, y la fabricación de desinfectantes y limpiadores de cocina. Pese a su gran uso, el amoníaco es cáustico, tóxico y peligroso. La producción industrial del amoníaco en 2012 fue de 198 000 000 toneladas, lo que equivale a un 35 % de incremento con respecto al año 2006, con 146 500 000 toneladas.[7]
 Estructura química | ||
 Estructura tridimensional | ||
| Nombre IUPAC | ||
| Azano | ||
| General | ||
| Otros nombres |
Hidruro de nitrógeno Trihidruro de nitrógeno Espíritus de Hartshorn | |
| Fórmula estructural |
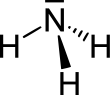 | |
| Fórmula molecular | NH3 | |
| Identificadores | ||
| Número CAS | 7664-41-7[1] | |
| Número RTECS |
BO0875000 (anhidro) BQ9625000 (soluciones) | |
| ChEBI | 16134 | |
| ChEMBL | CHEMBL1160819 | |
| ChemSpider | 217 | |
| DrugBank | DB11118 | |
| PubChem | 134988186 | |
| UNII | 5138Q19F1X | |
| KEGG | C00014 D02916, C00014 | |
| Propiedades físicas | ||
| Apariencia |
Incoloro Olor penetrante y desagradable | |
| Densidad | 0,723 kg/m³; 0,000723 g/cm³ | |
| Masa molar | 17,021 g/mol | |
| Punto de fusión | 195,42 K (−78 °C) | |
| Punto de ebullición | 239,81 K (−33 °C) | |
| Punto de descomposición | 773 K (500 °C) <head> | |
| Temperatura crítica | 405,5 K (132 °C) | |
| Presión crítica | 111.52 atm | |
| Índice de refracción (nD) | 1.355 | |
| Propiedades químicas | ||
| Acidez | 9.24[2] pKa | |
| Alcalinidad | 5[3] pKb | |
| Solubilidad en agua | 89.9 g/100 ml (0 °C) | |
| Momento dipolar | 1.42 D | |
| Familia | 15 | |
| Termoquímica | ||
| ΔfH0gas | -45.92 kJ/mol | |
| ΔfH0líquido | -40.2 kJ/mol | |
| S0gas, 1 bar | 192.77 J·mol–1·K | |
| Capacidad calorífica (C) |
4700 kJ/kg·K (liq) 80.08 J/mol·K | |
| Peligrosidad | ||
| SGA |
    | |
| Punto de inflamabilidad | 284 K (11 °C) | |
| NFPA 704 |
1
3
0
| |
| Temperatura de autoignición | 924 K (651 °C) | |
| Frases R | R10, R23, R34, R50 | |
| Frases S | (S1/2), S9, S16, S26, S36/37/39, S45, S61 | |
| Frases H | H221, H314, H331, H400 | |
| Límites de explosividad | 15–28 %[4] | |
| Riesgos | ||
| Ingestión | Es peligroso. Síntomas incluyen náusea y vómitos, daño a los labios, boca y esófago. | |
| Inhalación | Los vapores son extremadamente irritantes y corrosivos. | |
| Piel | Disoluciones concentradas pueden producir quemaduras severas y necrosis. | |
| Ojos | Puede causar daños permanentes, incluso en cantidades pequeñas. | |
| Más información | Hazardous Chemical Database | |
| Compuestos relacionados | ||
| Hidruros relacionados |
Arsina Fosfina Estibina Bismutina | |
| Hidruros de nitrógeno relacionados |
Hidrazina Ácido azothídrico | |
| Otros compuestos | Hidróxido de amonio | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El NH3 hierve a los -33.34 °C a una presión de una atmósfera, esto ayuda a que pueda conservarse en estado líquido, bajo presión a temperaturas bajas. Sin embargo, a temperaturas mayores a 405.5 K (temperatura crítica) ningún aumento en la presión producirá la condensación de este gas. Si la presión aumenta por encima del valor crítico de 111.5 atm, cualquier aumento por encima de este valor aumenta la compresión de las moléculas del gas, pero no se forma una fase líquida definida. El amoníaco casero o hidróxido de amonio (NH4OH), es una solución de NH3 en agua. La concentración de dicha solución es medida en unidades de la Escala Baumé, con 26 grados baumé (cerca del 30 % por peso de amoníaco) como concentración típica del producto comercial.[8]
Según la teoría de repulsión entre pares de electrones de la capa de valencia, los pares electrónicos de valencia del nitrógeno en la molécula se orientan hacia los vértices de un tetraedro, distribución característica cuando existe hibridación sp³. Existe un par solitario, por lo que la geometría de la molécula es piramidal trigonal (grupo puntual de simetría C3v). En disolución acuosa se puede comportar como una base y formarse el ion amonio, NH4+, con un átomo de hidrógeno en cada vértice de un tetraedro.
El amoníaco, a temperatura ambiente, es un gas incoloro de olor muy penetrante y nauseabundo. Se produce naturalmente por descomposición de la materia orgánica y también se fabrica industrialmente. Es fácilmente soluble y se evapora rápidamente. Generalmente se vende en forma líquida.
La cantidad de amoníaco producido industrialmente cada año es casi igual a la producida por la naturaleza. El amoníaco es producido naturalmente en el suelo por bacterias, por plantas y animales en descomposición y por desechos animales. El amoníaco es esencial para muchos procesos biológicos.
La mayor parte (más del 80 %) del amoníaco producido en plantas químicas es usada para fabricar abonos y para su aplicación directa como abono. El resto es usado en textiles, plásticos, explosivos, en la producción de pulpa y papel, alimentos y bebidas, productos de limpieza domésticos, refrigerantes y otros productos. También se usa en sales aromáticas.
Por su pH alcalino, es capaz de reaccionar con ácidos produciendo sales de amonio.
Su nombre fue dado por el químico sueco Torbern Bergman (1735-1784) al gas obtenido en los depósitos de sal cerca del templo de Amón, en Libia (del griego: ἀμμωνιακόν [ammōniakón] ‘lo perteneciente a Amón’).[9][10]
