
Chlorure d'aluminium
composé chimique / De Wikipedia, l'encyclopédie encyclopedia
Cher Wikiwand IA, Faisons court en répondant simplement à ces questions clés :
Pouvez-vous énumérer les principaux faits et statistiques sur Chlorure d'aluminium?
Résumez cet article pour un enfant de 10 ans
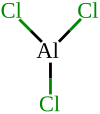
Le chlorure d'aluminium (AlCl3) aussi appelé trichlorure d’aluminium, ou chlorure d'aluminium(III), est un sel d'aluminium et de chlore. La forme anhydre possède une structure particulière : bien qu'étant un halogénure d'un métal très électropositif, les liaisons chimiques sont principalement covalentes et non pas ioniques comme on pourrait s'y attendre. Cela a notamment pour conséquence qu'AlCl3 possède des températures de fusion et de sublimation basses (178 °C pour cette dernière), et qu'à l'état liquide, il conduit mal l'électricité contrairement aux halogénures ioniques comme le chlorure de sodium. Ce composé existe à l'état solide sous la forme d'un réseau hexacoordiné. Il fond en formant un dimère tétracoordiné, Al2Cl6 qui peut se vaporiser, mais qui se dissocie à température plus élevée pour former une espèce AlCl3 analogue à BF3.
| Chlorure d'aluminium(III) | |||||
   |
|||||
| Identification | |||||
|---|---|---|---|---|---|
| Nom UICPA | trichloroalumane | ||||
| Synonymes |
trichlorure d'aluminium |
||||
| No CAS | 7446-70-0 | ||||
| No ECHA | 100.028.371 | ||||
| No CE | 231-208-1 | ||||
| No RTECS | BD0525000 | ||||
| Code ATC | D10AX01 | ||||
| PubChem | 24012 | ||||
| SMILES | |||||
| InChI | |||||
| Apparence | solide jaune pâle | ||||
| Propriétés chimiques | |||||
| Formule | AlCl3 [Isomères] |
||||
| Masse molaire[1] | 133,341 ± 0,006 g/mol Al 20,23 %, Cl 79,76 %, |
||||
| Propriétés physiques | |||||
| T° fusion | 190 °C[réf. souhaitée] | ||||
| T° ébullition | 182,7 °C à 752 mmHg (sublimation)[2] | ||||
| Solubilité | dans l'eau : 439 g l−1 (0 °C), 449 g l−1 (10 °C), 458 g l−1 (20 °C) 466 g l−1 (30 °C) 473 g l−1 (40 °C) 481 g l−1 (60 °C) 486 g l−1 (80 °C) 490 g l−1 (100 °C). éthanol : 1 000 g l−1 (12,5 °C). chloroforme : 0,7 g l−1 (20 °C). CCl4 : soluble. éther : soluble[réf. souhaitée] |
||||
| Masse volumique | 2,44 à 2,48 g/cm3[2] | ||||
| Point critique | 26,3 bar, 346,85 °C[3] | ||||
| Cristallographie | |||||
| Système cristallin | Monoclinique | ||||
| Réseau de Bravais | mC | ||||
| Symbole de Pearson |  [4] [4]
|
||||
| Classe cristalline ou groupe d’espace | C2/m (no 12)[4] | ||||
| Strukturbericht | D015[4] | ||||
| Structure type | YCl3 | ||||
| Précautions | |||||
| SGH[5] | |||||
| H314 H314 : Provoque de graves brûlures de la peau et des lésions oculaires |
|||||
| NFPA 704 | |||||
| Transport[2] | |||||
Code Kemler : 80 : matière corrosive ou présentant un degré mineur de corrosivité Numéro ONU : 1726 : CHLORURE D’ALUMINIUM ANHYDRE Classe : 8 Code de classification : C2 : Matières corrosives sans risque subsidiaire ; Matières de caractère acide: Inorganiques, solides ; Étiquette :  8 : Matières corrosives Emballage : Groupe d'emballage II : matières moyennement dangereuses ; Code Kemler : 80 : matière corrosive ou présentant un degré mineur de corrosivité Numéro ONU : 2581 : CHLORURE D’ALUMINIUM EN SOLUTION Classe : 8 Code de classification : C1 : Matières corrosives sans risque subsidiaire ; Matières de caractère acide: Inorganiques, liquides ; Étiquette :  8 : Matières corrosives Emballage : Groupe d'emballage III : matières faiblement dangereuses. |
|||||
| Écotoxicologie | |||||
| DL50 | 3 450 mg kg−1[réf. souhaitée] | ||||
| Unités du SI et CNTP, sauf indication contraire. | |||||
| modifier |
|||||
Le chlorure d'aluminium est très déliquescent et il peut exploser au contact de l'eau sous l'effet de l'hydratation. Il s'hydrolyse partiellement en présence d'eau pour former du chlorure d'hydrogène (acide chlorhydrique). En solution aqueuse, AlCl3 est totalement ionisé et la solution conduit bien le courant électrique. Cette solution est acide. De manière simplifiée, le cation produit par l'hydrolyse du chlorure d'aluminium s'écrit :
.
AlCl3 est probablement l'acide de Lewis le plus couramment utilisé et parmi les plus puissants. Ce composé possède de très nombreuses applications dans l'industrie chimique, notamment comme catalyseur pour les réactions de Friedel-Crafts, à la fois l'alkylation et l'acylation. Il est également utilisé pour des réactions de polymérisation ou d'isomérisation de composés organiques.
Il existe également un chlorure d'aluminium(I) (AlCl), mais il est très instable et n'est connu qu'à l'état gazeux.


![{\displaystyle {\ce {[Al(H2O)6]^3+ + H2O <=> [Al(H2O)5OH]^2+ + H3O+}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/ca99634e7b52aac56a62d879a5eccde92f41ea87)