Oxyde de vanadium(V)
composé chimique / De Wikipedia, l'encyclopédie encyclopedia
Cher Wikiwand IA, Faisons court en répondant simplement à ces questions clés :
Pouvez-vous énumérer les principaux faits et statistiques sur Pentoxyde de vanadium?
Résumez cet article pour un enfant de 10 ans
AFFICHER TOUTES LES QUESTIONS
Pour les articles homonymes, voir Oxyde de vanadium.
L'oxyde de vanadium(V) ou pentoxyde de vanadium (V2O5) est la forme la plus oxydée du vanadium.
Faits en bref Identification, Nom UICPA ...
| Pentoxyde de vanadium | |||

| |||
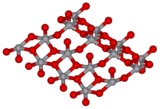 | |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | Oxyde de Vanadium (V) | ||
| Synonymes |
Pentoxyde de vanadium |
||
| No CAS | 1314-62-1 | ||
| No ECHA | 100.013.855 | ||
| No CE | 215-239-8 | ||
| SMILES | |||
| InChI | |||
| Apparence | poudre cristalline jaune à rouge ou solide de formes variables[1]. | ||
| Propriétés chimiques | |||
| Formule | O5V2V2O5 | ||
| Masse molaire[2] | 181,88 ± 0,001 7 g/mol O 43,98 %, V 56,02 %, |
||
| Propriétés physiques | |||
| T° fusion | 690 °C[1] | ||
| T° ébullition | (décomposition) : 1 750 °C[1] | ||
| Solubilité | dans l'eau : 8 g·l-1[1] | ||
| Masse volumique | 3,4 g·cm-3[1] | ||
| Thermochimie | |||
| S0solide | 130,4 J K−1 mol−1[3] | ||
| ΔfH0liquide | −1 491,2 kJ mol−1[3] | ||
| ΔfH0solide | −1 550,6 kJ mol−1[3] | ||
| Cp | 130,5 J K−1 mol−1 à 25°C[3] | ||
| Cristallographie | |||
| Système cristallin | Orthorhombique[4] | ||
| Classe cristalline ou groupe d’espace | Pmmn (no 59) orthorhombique Hermann-Mauguin :  |
||
| Paramètres de maille | a = 11,552 Å, b = 3,619 Å, c = 4,797 Å[4] | ||
| Précautions | |||
| SGH[5] | |||
| H302, H332, H335, H341, H361d, H372 et H411 H302 : Nocif en cas d'ingestion H332 : Nocif par inhalation H335 : Peut irriter les voies respiratoires H341 : Susceptible d'induire des anomalies génétiques (indiquer la voie d'exposition s'il est formellement prouvé qu'aucune autre voie d'exposition ne conduit au même danger) H361d : Susceptible de nuire au fœtus. H372 : Risque avéré d'effets graves pour les organes (indiquer tous les organes affectés, s'ils sont connus) à la suite d'expositions répétées ou d'une exposition prolongée (indiquer la voie d'exposition s'il est formellement prouvé qu'aucune autre voie d'exposition ne conduit au même danger) H411 : Toxique pour les organismes aquatiques, entraîne des effets à long terme |
|||
| Transport | |||
|
|||
| Classification du CIRC | |||
| Groupe 2B : Peut-être cancérogène pour l'homme[6] | |||
| Unités du SI et CNTP, sauf indication contraire. | |||
| modifier |
|||
Fermer
On s'en sert comme catalyseur souvent sur un support d'alumine. Il est utilisé dans la synthèse de l'acide sulfurique où il catalyse l'oxydation du dioxyde de soufre en trioxyde.
C'est aussi un précurseur pour la production d'alliage de vanadium[7].




