
חומצה פלואורואנטימונית
תרכובת / ויקיפדיה האנציקלופדיה encyclopedia
חומצה פלואורואנטימונית, H2FSbF6, היא תערובת אנאורגנית של חומצה הידרופלואורית (HF) ואנטימון שש-פלואורי (SbF6) והיא מערכת הסופר-חומצה החזקה ביותר שנתגלתה. נוסחת החומצה ההידורפלואורית שנרשמת היא +H2F, כיוון שמתקיים קשר מימני בו נוצר קשר בין זוג אלקטרונים הבלתי קושרים של אטום הפלואור לאלקטרון הקושר של המימן (עקב הפרשי אלקטרושליליות). חומר זה נקרא גם פלואורוניום.
 | |
| חומצה פלואורית (Fluoronium) ואנטימון שש פולואורי | |
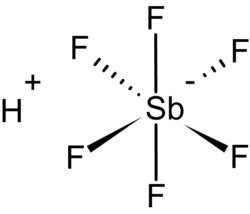 | |
| כתיב כימי |
HSbF₆ |
|---|---|
| מסה מולרית | 256.765 גרם/מול |
| מראה | נוזל חסר צבע |
| מספר CAS | 16950-06-4 |
| צפיפות | 2.885 g/cm3 גרם/סמ"ק |
| מצב צבירה | נוזל |
| מסיסות | SO2ClF, SO2 |
| NFPA 704 | |
במערכת החומצה הפלואורואנטימונית, החומצה הפלואורית משחררת פרוטון (+H) ונוצר הבסיס המוצמד (-F). יון הפלואוריד יוצר קשר קואורדנטיבי עם האנטימון החמש פלואורי.
הנוסחה לקבלת חומצה פלואורואנטימונית היא:
- -2HF ⇌ H2F+ + F
- SbF5 + F− → SbF6
- ניסוח נטו:
- +SbF5-+2HF+→SbF6-+H2F
- ניסוח הנטו אינו בשיווי משקל והתגובה היא אקסותרמית.
- חומצה זו ידועה לשמצה בשל חוזקה לשבור קשרים פחמימנים.
התוצאה של תהליך זה הוא פרוטון חופשי ואניון אוקטאהדרלי של אנטימון שש פלואורי.
האנטימון שש-פלואורי הוא נוקלאופיל חלש ואחד הבסיסים החלשים ביותר שקיימים. הפרוטון החופשי שנוצר בעת תהליך המערכת הוא זה שהופך את המערכת לחומצית במידה מדהימה.
החומצה הפלואורואנטימונית היא חזקה פי 2x1019 (עשרים קוונטיליון) מחומצה גופרתית בריכוז של 100%.[1] את הדיסוציאציה האוטומטית של החומצה הפלואורו אנטימונית ניתן לתאר כך:

