
ヒストン修飾酵素
ウィキペディア フリーな encyclopedia
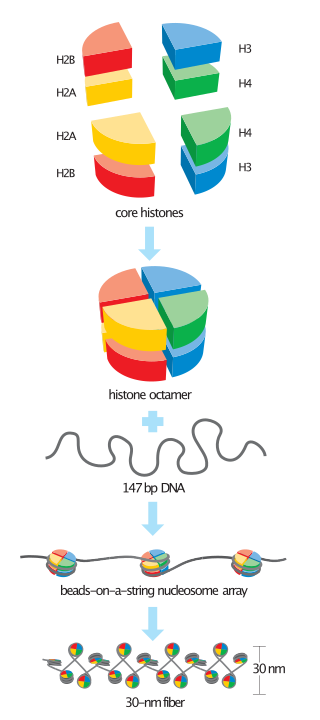
ヒストン修飾酵素(ヒストンしゅうしょくこうそ、英: histone-modifying enzyme)は、ヒストンタンパク質に対する翻訳後修飾に関与する酵素の総称である[1]。真核生物のゲノムを安全に保管するため、DNAは4種類のコアヒストンタンパク質(H2A、H2B、H3、H4)に巻き付き、ヌクレオソームを形成している。こうしたヌクレオソームはさらに、高度に凝縮したクロマチンへと折りたたまれ、転写、複製、組換え、修復に必要な因子は遺伝物質にアクセスできないようになっている[2][3]。真核生物は、このクロマチンによる抑制的な障壁に対し、ヒストン修飾を介して克服する複雑な機構を発達させている。ヒストン修飾は、ヒストンの残基に特定の官能基を共有結合的に付加する翻訳後修飾である。ヒストンに付加された官能基は、緩く開いたクロマチン構造であるユークロマチン、もしくは固く閉じたクロマチン構造であるヘテロクロマチンのいずれかの状態を直接的または間接的に引き出す。ユークロマチンは活発な転写と遺伝子発現の標識であり、ヒストンのパッキングは軽度であるため転写過程に関与するタンパク質が進入することが可能である。一方で固くパッキングしたヘテロクロマチンは、現在遺伝子発現が行われていないことの標識となる[3]。

ヒストンに対する翻訳後修飾にはいくつかの異なる種類が存在するが、最も一般的な修飾は、アセチル化[4]、メチル化[5]、リン酸化[6]、ユビキチン化[7]の4種類である。修飾を誘導する酵素(官能基の付加など)はライター(writer)と呼ばれ、修飾を除去する酵素はイレイサー(eraser)と呼ばれる。さらに、O-GlcNAc化[8]、SUMO化[9]、ADPリボシル化[10]、シトルリン化[11][12]、プロリンの異性化[13]など、稀な修飾も多くの種類が存在する。