
Ácido sulfúrico
composto físico / De Wikipedia, a enciclopédia encyclopedia
Ácido sulfúrico, também conhecido como vitríolo, é um ácido mineral composto pelos elementos enxofre, oxigênio e hidrogênio com a fórmula molecular H2SO4. É um líquido viscoso, incolor, inodoro e solúvel em água, produzindo uma reação altamente exotérmica.[4]
| Ácido sulfúrico Alerta sobre risco à saúde | |
|---|---|
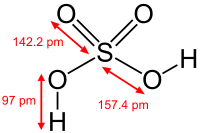 | |
 | |
 | |
| Nome IUPAC | Ácido sulfúrico |
| Outros nomes | Óleo de vitriolo |
| Identificadores | |
| Número CAS | 7664-93-9 |
| Número EINECS | 231-639-5 |
| Número RTECS | WS5600000 |
| Propriedades | |
| Fórmula molecular | H2SO4 |
| Massa molar | 98.078 g/mol |
| Aparência | Líquido, límpido, incolor e inodoro. |
| Densidade | 1,8356 g·cm-3, líquido[1] |
| Ponto de fusão |
10,38 °C (100 %) [1] |
| Ponto de ebulição |
337 °C (100 %) [1] |
| Solubilidade em água | completamente miscível [1] |
| Pressão de vapor | 1,3 hPa (145,8 °C) [1] |
| Acidez (pKa) | -3,9[2] 1,96[2] |
| Viscosidade | 23,55 cP (20 °C); |
| Riscos associados | |
| MSDS | ICSC 0362 |
| Classificação UE | |
| Índice UE | 016-020-00-8 |
| NFPA 704 | |
| Frases R | R35 |
| Frases S | S1/2, S26, S30, S45 |
| Ponto de fulgor | Não inflamável |
| LD50 | 2140 mg·kg-1 (Rato, oral)[3] |
| Compostos relacionados | |
| Outros aniões/ânions | Ácido sulfâmico (um -OH substituído por -NH2) Ácido fluorossulfúrico (um -OH substituído por -F) |
| Outros catiões/cátions | Sulfato de lítio |
| Ácidos fortes relacionados | Ácido selênico Ácido clorídrico Ácido nítrico |
| Compostos relacionados | Ácido sulfuroso Ácido peroxisulfúrico Óxido sulfúrico Oleum Ácido tiossulfúrico (um =O substituído por =S) |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Sua corrosividade pode ser atribuída principalmente à sua natureza de ácido forte e, se em alta concentração, a suas propriedades de desidratação e oxidação. Também é higroscópico, prontamente absorvendo vapor d'água do ar.[4] Em contato com a pele o ácido sulfúrico pode causar graves queimaduras químicas e até queimaduras de segundo grau; é muito perigoso mesmo em concentrações moderadas.[5][6]
O ácido sulfúrico é um importante produto e, de fato, a produção de ácido sulfúrico de um país é um bom indicador de sua força industrial.[7] É largamente produzido por diferentes métodos, como o processo de contato, o processo de ácido sulfúrico a úmido, o processo de câmara de chumbo e alguns outros métodos.[8]
O uso mais comum de ácido sulfúrico (60% do total) é na a indústria de fertilizantes.[9] Também é uma substância essencial para a indústria química. Os usos principais incluem produção de fertilizantes (e outros processamentos minerais), refinamento de petróleo, tratamento de águas residuais e síntese química. Possui um vasto uso de aplicações finais, como em eletrólitos de baterias de chumbo-ácido e em vários agentes de limpeza.
