鎵(英語:Gallium),是一種化學元素,化學符號为Ga,原子序數为31,原子量為7001697230000000000♠69.723 u,位於元素週期表的第13族,為一種貧金屬,與同族的鋁、銦和鉈具有相似的特性。它是由法国化学家保罗·埃米尔·勒科克·德布瓦博德兰在1875年发现的。[8]
事实速览 外觀, 概況 ...
镓 31Ga|
|
| 外觀 |
|---|
蓝银色金属
 |
| 概況 |
|---|
| 名稱·符號·序數 | 镓(gallium)·Ga·31 |
|---|
| 元素類別 | 贫金属 |
|---|
| 族·週期·區 | 13·4·p |
|---|
| 標準原子質量 | 69.723(1)[1] |
|---|
| 电子排布 | [Ar] 3d104s24p1
2, 8, 18, 3
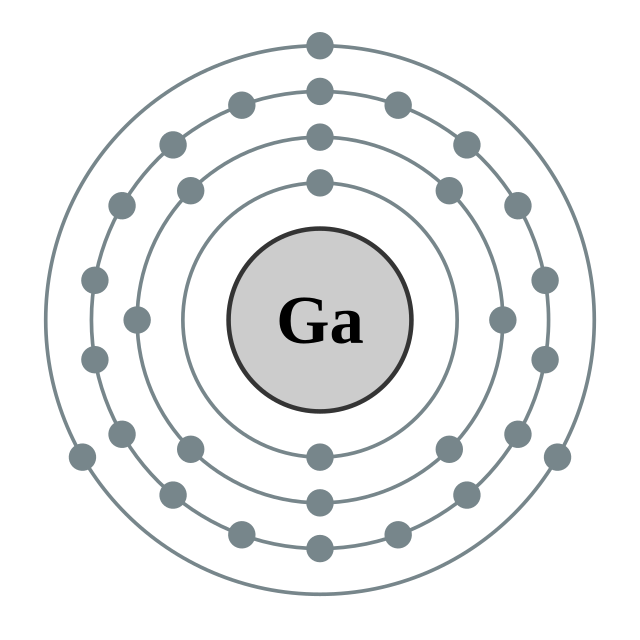 镓的电子層(2, 8, 18, 3) 镓的电子層(2, 8, 18, 3) |
|---|
| 歷史 |
|---|
| 預測 | 德米特里·门捷列夫(1871年) |
|---|
| 發現 | 保罗·埃米尔·勒科克·德布瓦博德兰(1875年) |
|---|
| 分離 | 保罗·埃米尔·勒科克·德布瓦博德兰(1875年) |
|---|
| 物理性質 |
|---|
| 物態 | 固态 |
|---|
| 密度 | (接近室温)
5.91 g·cm−3 |
|---|
| 熔点時液體密度 | 6.095 g·cm−3 |
|---|
| 熔点 | 302.9146 K,29.7646 °C,85.5763 °F |
|---|
| 沸點 | 2673 K,2400 °C,4352[2] °F |
|---|
| 熔化热 | 5.59 kJ·mol−1 |
|---|
| 汽化热 | 254 kJ·mol−1 |
|---|
| 比熱容 | 25.86 J·mol−1·K−1 |
|---|
蒸氣壓
| 壓/Pa
|
1
|
10
|
100
|
1 k
|
10 k
|
100 k
|
| 溫/K
|
1310
|
1448
|
1620
|
1838
|
2125
|
2518
|
|
| 原子性質 |
|---|
| 氧化态 | −5, −4, −3,[3] −2, −1, 0, +1, +2, +3[4]
(两性) |
|---|
| 电负性 | 1.81(鲍林标度) |
|---|
| 电离能 | 第一:578.8 kJ·mol−1
第二:1979.3 kJ·mol−1
第三:2963 kJ·mol−1
(更多) |
|---|
| 原子半径 | 135 pm |
|---|
| 共价半径 | 122±3 pm |
|---|
| 范德华半径 | 187 pm |
|---|
 镓的原子谱线 镓的原子谱线 |
| 雜項 |
|---|
| 晶体结构 | 正交 |
|---|
| 磁序 | 抗磁性 |
|---|
| 磁化率 | 3004784000000000000♠−21.6×10−6 cm3/mol (当290 K)[5] |
|---|
| 电阻率 | 140 n[6] Ω·m |
|---|
| 熱導率 | 40.6 W·m−1·K−1 |
|---|
| 膨脹係數 | (25 °C)18 µm·m−1·K−1 |
|---|
| 聲速(細棒) | (20 °C)2740 m·s−1 |
|---|
| 杨氏模量 | 9.8 GPa |
|---|
| 泊松比 | 0.47 |
|---|
| 莫氏硬度 | 1.5 |
|---|
| 布氏硬度 | 60 MPa |
|---|
| CAS号 | 7440-55-3 |
|---|
| 同位素 |
|---|
主条目:镓的同位素
|
关闭
在標準狀況下,鎵元素是質地柔軟的銀色金屬,在液态下則為银白色。如果对镓施加太多力,它就可能形成贝壳状断口。自1875年發現以來,鎵一直被用於製造低熔點合金。它還用於半導體基材的摻雜劑。
鎵的熔點可作為溫度參考點。鎵合金亦可應用於溫度計,作為代替汞的無毒和環保的替用品,並且可以承受比汞更高的溫度。鎵銦錫合金(62–95%鎵,5–22%銦和0–16%錫)具有遠低於水凝固點的凝固點−19 °C(−2 °F),但这也可能是过冷的凝固點。
镓在自然界中不以单质存在,常以镓(III)的形式微量散存於鋅礦(例如闪锌矿)、鋁土礦等礦石中。镓在29.76 °C(85.57 °F)会融化成液體,因此會融化於人的手中(一般人的體溫為37.0 °C(98.6 °F))。
鎵在多種關鍵新興技術中皆有重要應用。電子設備中主要使用的鎵化合物砷化鎵,用於微波電路、高速轉換電路、紅外線電路。半導體氮化鎵和氮化銦鎵则用於製造藍色和紫色的發光二極體(LED)和雷射二極體。除此之外,鎵也用於生產珠寶用途的人造釓鎵榴石型鐵氧體。镓被列為一種技术关键元素。[9][10]
鎵在生物學中沒有已知的天然作用。三價鎵和三價鐵在生物系統中有相似的作用,因此三價鎵也被應用在藥學和放射藥理學上。



