
সোডিয়াম কার্বনেট
রাসায়নিক যৌগ / From Wikipedia, the free encyclopedia
সোডিয়াম বাইকার্বনেট (বেকিং সোডা), একটি অনুরূপ যৌগের নিবন্ধের সাথে বিভ্রান্ত হবেন না।
সোডিয়াম কার্বনেট (ওয়াশিং সোডা, সোডা অ্যাশ এবং সোডা স্ফটিক নামেও পরিচিত) হল Na2CO3 এবং এর বিভিন্ন হাইড্রেটের সূত্র সহ অজৈব যৌগ। সোডিয়াম কার্বনেটের সব রূপই সাদা বর্ণের। ভৌত ধর্মের দিক থেকে এটি গন্ধহীন এবং জলে দ্রাব্য। জলে দ্রবীভূত হয়ে এটি ক্ষারীয় দ্রবণ তৈরি করে।
এই নিবন্ধটি ইংরেজি থেকে আনাড়িভাবে অনুবাদ করা হয়েছে। এটি কোনও কম্পিউটার কর্তৃক অথবা দ্বিভাষিক দক্ষতাহীন কোনো অনুবাদক কর্তৃক অনূদিত হয়ে থাকতে পারে। |
দ্রুত তথ্য নামসমূহ, শনাক্তকারী ...
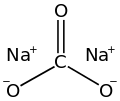 | |
 | |
| নামসমূহ | |
|---|---|
| ইউপ্যাক নাম
সোডিয়াম কার্বনেট | |
| পছন্দসই ইউপ্যাক নাম
Disodium carbonate | |
| অন্যান্য নাম
Soda ash, washing soda, soda crystals, sodium trioxocarbonate | |
| শনাক্তকারী | |
ত্রিমাত্রিক মডেল (জেমল) |
|
| সিএইচইবিআই | |
| সিএইচইএমবিএল | |
| কেমস্পাইডার |
|
| ইসিএইচএ ইনফোকার্ড | ১০০.০০৭.১২৭ |
| ইসি-নম্বর |
|
| ই নম্বর | E৫০০(i) (অম্লতা নিয়ন্ত্রক, ...) |
পাবকেম CID |
|
| আরটিইসিএস নম্বর |
|
| ইউএনআইআই |
|
কম্পটক্স ড্যাশবোর্ড (EPA) |
|
| |
এসএমআইএলইএস
| |
| বৈশিষ্ট্য | |
| Na2CO3 | |
| আণবিক ভর | 105.9888 g/mol (anhydrous) 286.1416 g/mol (decahydrate) |
| বর্ণ | White solid, hygroscopic |
| গন্ধ | Odorless |
| ঘনত্ব | |
| গলনাঙ্ক | ৮৫১ °সে (১,৫৬৪ °ফা; ১,১২৪ K) (Anhydrous) ১০০ °সে (২১২ °ফা; ৩৭৩ K) decomposes (monohydrate) ৩৩.৫ °সে (৯২.৩ °ফা; ৩০৬.৬ K) decomposes (heptahydrate) ৩৪ °সে (৯৩ °ফা; ৩০৭ K) (decahydrate)[2][3] |
পানিতে দ্রাব্যতা |
Anhydrous, g/100 mL:
|
| দ্রাব্যতা | Soluble in aq. alkalis,[4] glycerol Slightly soluble in aq. alcohol Insoluble in CS2, acetone, alkyl acetates, alcohol, benzonitrile, liquid ammonia[5] |
| দ্রাব্যতা in glycerine | 98.3 g/100 g (155 °C)[5] |
| দ্রাব্যতা in ethanediol | 3.46 g/100 g (20 °C)[6] |
| দ্রাব্যতা in dimethylformamide | 0.5 g/kg[6] |
| অম্লতা (pKa) | 10.33 [7] |
চৌম্বকক্ষেত্রের প্রতি সংবেদনশীলতা (χ) |
−4.1·10−5 cm3/mol[2] |
| প্রতিসরাঙ্ক (nD) | 1.485 (anhydrous) 1.420 (monohydrate)[3] 1.405 (decahydrate) |
| সান্দ্রতা | 3.4 cP (887 °C)[6] |
| গঠন | |
| স্ফটিক গঠন | Monoclinic (γ-form, β-form, δ-form, anhydrous)[8] Orthorhombic (monohydrate, heptahydrate)[1][9] |
| Space group | C2/m, No. 12 (γ-form, anhydrous, 170 K) C2/m, No. 12 (β-form, anhydrous, 628 K) P21/n, No. 14 (δ-form, anhydrous, 110 K)[8] Pca21, No. 29 (monohydrate)[1] Pbca, No. 61 (heptahydrate)[9] |
| Point group | 2/m (γ-form, β-form, δ-form, anhydrous)[8] mm2 (monohydrate)[1] 2/m 2/m 2/m (heptahydrate)[9] |
| Lattice constant | |
| Coordination geometry |
Octahedral (Na+, anhydrous) |
| তাপ রসায়নবিদ্যা | |
| তাপ ধারকত্ব, C | 112.3 J/mol·K[2] |
| স্ট্যন্ডার্ড মোলার এন্ট্রোফি এস |
135 J/mol·K[2] |
| গঠনে প্রমান এনথ্যাল্পির পরিবর্তন ΔfH |
−1130.7 kJ/mol[2][6] |
গিবসের মুক্ত শক্তি (ΔfG˚) |
−1044.4 kJ/mol[2] |
| ঝুঁকি প্রবণতা | |
| প্রধান ঝুঁকিসমূহ | Irritant |
| নিরাপত্তা তথ্য শীট | MSDS |
| জিএইচএস চিত্রলিপি |  [10] [10] |
| জিএইচএস সাংকেতিক শব্দ | সতর্কতা |
| জিএইচএস বিপত্তি বিবৃতি | H319[10] |
| জিএইচএস সতর্কতামূলক বিবৃতি | P305+351+338[10] |
| এনএফপিএ ৭০৪ | 
২
০ |
| প্রাণঘাতী ডোজ বা একাগ্রতা (LD, LC): | |
LD৫০ (মধ্যমা ডোজ) |
4090 mg/kg (rat, oral)[12] |
| সম্পর্কিত যৌগ | |
অন্যান্য অ্যানায়নসমূহ |
Sodium bicarbonate |
অন্যান্য ক্যাটায়নসমূহ |
Lithium carbonate Potassium carbonate Rubidium carbonate Cesium carbonate |
সম্পর্কিত যৌগ |
Sodium sesquicarbonate Sodium percarbonate |
সুনির্দিষ্টভাবে উল্লেখ করা ছাড়া, পদার্থসমূহের সকল তথ্য-উপাত্তসমূহ তাদের প্রমাণ অবস্থা (২৫ °সে (৭৭ °ফা), ১০০ kPa) অনুসারে দেওয়া হয়েছে। | |
| তথ্যছক তথ্যসূত্র | |
বন্ধ
সোডিয়াম কার্বোনেট সর্বপ্রথম সোডিয়াম সমৃদ্ধ মাটিতে জন্মানো উদ্ভিদের ছাই থেকে বের করা হয়েছিল। কারণ এই সোডিয়াম-সমৃদ্ধ উদ্ভিদের ছাই কাঠের ছাই থেকে লক্ষণীয়ভাবে আলাদা ছিল (একসময় পটাশ উৎপাদনের জন্য ব্যবহৃত হত), সোডিয়াম কার্বনেট "সোডা অ্যাশ" নামে পরিচিত হয়ে ওঠে। [সম্পূর্ণ উদ্ধৃতি প্রয়োজন] এটি সোডিয়াম ক্লোরাইড এবং চুনাপাথর থেকে সোলভে প্রক্রিয়ার মাধ্যমে প্রচুর পরিমাণে উত্পাদিত হয়, সেইসাথে কার্বনেট সোডিয়াম হাইড্রক্সাইড যা ক্লোর-ক্ষার প্রক্রিয়া ব্যবহার করে তৈরি করা হয়।