
Bicarbonate
anion / De Wikipedia, l'encyclopédie encyclopedia
Cher Wikiwand IA, Faisons court en répondant simplement à ces questions clés :
Pouvez-vous énumérer les principaux faits et statistiques sur Bicarbonate?
Résumez cet article pour un enfant de 10 ans
Le bicarbonate, ou hydrogénocarbonate, est un ion polyatomique dont la formule chimique est HCO3−. Le bicarbonate doit son préfixe (« bi- ») à son double caractère acido-basique (dit caractère amphotère) : il est à la fois acide et base, appartenant à deux couples acido-basiques différents. Il s'agit de la forme intermédiaire dans la double déprotonation de l'acide carbonique : ôter le premier proton (ion H+) de l'acide carbonique donne le bicarbonate ; ôter le second proton donnera la forme carbonate ionique.
| Bicarbonate | |
 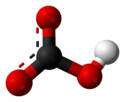 Structure de l'ion bicarbonate. |
|
| Identification | |
|---|---|
| Nom UICPA | hydrogénocarbonate |
| No CAS | 71-52-3 |
| PubChem | 769 |
| ChEBI | 17544 |
| SMILES | |
| InChI | Std. InChI : vue 3D InChI=1S/CH2O3/c2-1(3)4/h(H2,2,3,4)/p-1 Std. InChIKey : BVKZGUZCCUSVTD-UHFFFAOYSA-M |
| Propriétés chimiques | |
| Formule | CHO3HCO3 |
| Masse molaire[1] | 61,016 8 ± 0,001 8 g/mol C 19,68 %, H 1,65 %, O 78,66 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le mot s'écrit au pluriel (bicarbonates) lorsqu'il s'agit des sels de l'ion bicarbonate : par exemple, le bicarbonate de sodium (souvent appelé « bicarbonate de soude » par abus de langage, ou « soda à pâte » et « petite vache » au Canada) de formule NaHCO3, qui est le sel de l'ion bicarbonate le plus répandu et le plus utilisé. Il contribue à la digestion par notre organisme.