
Αμμωνία
χημική ένωση αζώτου και υδρογόνου, με χημικό τύπο NH3 / From Wikipedia, the free encyclopedia
Η αμμωνία[1] (αγγλικά: ammonia) είναι ανόργανη δυαδική χημική ένωση που περιέχει άζωτο και υδρογόνο, με μοριακό τύπο NH3. Η χημικά καθαρή αμμωνία, στις κανονικές συνθήκες περιβάλλοντος, δηλαδή σε θερμοκρασία 25°C και υπό πίεση 1 atm, είναι άχρωμο αέριο, με χαρακτηριστική αποπνικτική οσμή. Είναι το απλούστερο αζάνιο. Η αμμωνία (άμεσα ή έμμεσα) συνεισφέρει σημαντικά στις θρεπτικές ανάγκες των γήινων οργανισμών, εξυπηρετώντας ως πρόδρομη ένωση για τροφές και λιπάσματα. Επίσης, η αμμωνία αποτελεί δομικό συστατικό για τη σύνθεση πολλών φαρμακευτικών, αλλά και πολλών εμπορικών καθαριστικών προϊόντων. Παρά την ευρύτατη χρήση της, η ίδια η αμμωνία είναι καυστική και βλαβερή.
| Αμμωνία | |||
|---|---|---|---|
 | |||
 | |||
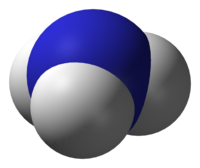 | |||
| Γενικά | |||
| Όνομα IUPAC | Αζάνιο | ||
| Άλλες ονομασίες | Αμμωνία Αζίδιο του υδρογόνου | ||
| Χημικά αναγνωριστικά | |||
| Χημικός τύπος | NH3 | ||
| Μοριακή μάζα | 17,031amu | ||
| Αριθμός CAS | 7664-41-7 | ||
| SMILES | N | ||
| InChI | 1/H3N/h1H3 | ||
| Αριθμός EINECS | 231-635-3 | ||
| Αριθμός RTECS | BO0875000 | ||
| Αριθμός UN | 1005 (άνυδρη) 2672 (διαλύματα) 2073 3318 | ||
| PubChem CID | 222 | ||
| ChemSpider ID | 217 | ||
| Δομή | |||
| Διπολική ροπή | 1,46 D | ||
| Μήκος δεσμού | 101,2 pm | ||
| Είδος δεσμού | πολωμένος ομοιοπολικός τύπου σ (1s-2sp³) | ||
| Γωνία δεσμού | 106,7˚ | ||
| Μοριακή γεωμετρία | τριγωνική πυραμιδική | ||
| Φυσικές ιδιότητες | |||
| Σημείο τήξης | −77,73 °C | ||
| Σημείο βρασμού | −33,34 °C | ||
| Κρίσιμη θερμοκρασία | 132,3°C | ||
| Κρίσιμη πίεση | 11,300 MPa | ||
| Πυκνότητα | 817 kg/m³ (-80°C, διαφανές στερεό) 860 kg/m³ (Σ.Ζ, 1,015 bar) 681,9 kg/m³ (-33,3°C, υγρό) 0,789 kg/m³ (Κ.Σ.) 0,73 kg/m³ (15°C) | ||
| Διαλυτότητα στο νερό | 47% w/w (0˚C) 31% w/w (25˚C) 18% w/w (50˚C) | ||
| Ιξώδες | 0,276 cP (−40 °C) | ||
| Δείκτης διάθλασης , nD | 1,3327 | ||
| Εμφάνιση | Άχρωμο αέριο | ||
| Χημικές ιδιότητες | |||
| pKa | 9,25 (  ) )38 (  ) ) | ||
| Σημείο αυτανάφλεξης | 651 °C | ||
| Επικινδυνότητα | |||
| Τοξική (T) Διαβρωτική (C) Βλαβερή για το Περιβάλλον (N) | |||
| Φράσεις κινδύνου | 10, 23, 34, 50 | ||
| Φράσεις ασφαλείας | (1/2), 9, 16, 26 36/37/39, 45, 61 | ||
| Κίνδυνοι κατά NFPA 704 | |||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||
Ταξινομήθηκε στις εξαιρετικά βλαβερές ουσίες στις ΗΠΑ (και όχι μόνο) και γι' αυτό οι εγκαταστάσεις που παράγουν, αποθηκεύουν ή χρησιμοποιούν αμμωνία σε σημαντικές ποσότητες υπόκεινται (νομικά) σε αυστηρώς απαιτούμενες προδιαγραφές ασφαλείας.[2]
Η παγκόσμια βιομηχανική παραγωγή αμμωνίας το 2014 ήταν 176.300.000 τόνοι.[3] δηλαδή είχε μια αύξηση της τάξης του 16% σε σχέση με το 2006, κατά το οποίο η παγκόσμια βιομηχανική παραγωγή αμμωνίας ήταν 152.000.000 τόνοι.[4]
Η (χημικά καθαρή) αμμωνία συχνά αποκαλείται «άνυδρη αμμωνία». Ο όρος δίνει έμφαση στην απουσία νερού από το υλικό. Η άνυδρη, λοιπόν, αμμωνία βράζει στους -33,34 °C (υπό πίεση 1 atm) οπότε όταν είναι υγρό πρέπει να αποθηκευθεί κάτω από υψηλή πίεση ή και σε ψύξη σε (αρκετά) χαμηλή θερμοκρασία. Σε αντιδιαστολή, το υδατικό διάλυμά της, που συχνά παριστάνεται με τον τύπο NH4OH, ο οποίος είναι ισοδύναμος με τον τύπο NH3 (aq), και αποκαλείται «οικιακή αμμωνία». Ένα τυπικό εμπορικό προϊόν «πυκνής αμμωνίας» αντιστοιχεί σε περίπου 30% (άνυδρη) αμμωνία (κατά μάζα)[5].
Ουσίες που περιέχουν αμμωνία ή και κάποια παρόμοια χημικά είδη (συνήθως το κατιόν του αμμωνίου, NH4+) συχνά αποκαλούνται με τη χρήση του επιθέτου «αμμωνιακός».
Επίσης το συστηματικό όνομα «αζάνιο», επεκτείνεται τόσο στην ομώνυμη ομόλογη σειρά, όσο και ευρύτερα ακόμη, δηλαδή και σε μια σειρά «θυγατρικών» αζωτούχων ανόργανων και οργανικών ενώσεων, που συμπεριλαμβάνουν και τις αμίνες.
