
Peróxido de hidrógeno
compuesto químico / De Wikipedia, la enciclopedia encyclopedia
Estimado Wikiwand AI, Seamos breves simplemente respondiendo estas preguntas clave:
¿Puede enumerar los principales datos y estadísticas sobre Peróxido de hidrógeno?
Resumir este artículo para un niño de 10 años
El peróxido de hidrógeno (H2O2), también conocido como agua oxigenada, dioxogen, dioxidano o peróxido de dihidrógeno es un compuesto químico con características de un líquido altamente polar, fuertemente enlazado con el hidrógeno, tal como el agua, por lo general de aspecto líquido ligeramente más viscoso. Es conocido por ser un poderoso oxidante.
 | ||
 | ||
| Nombre IUPAC | ||
| Peróxido de dihidrógeno | ||
| General | ||
| Otros nombres |
Agua oxigenada Dioxidano peróxido de dihidrogeno | |
| Fórmula estructural |
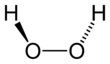 | |
| Fórmula molecular | H2O2 | |
| Identificadores | ||
| Número CAS | 7722-84-1[1] | |
| Número RTECS | MX0900000 | |
| ChEBI | 16240 | |
| ChEMBL | CHEMBL71595 | |
| ChemSpider | 763 | |
| DrugBank | 11091 | |
| PubChem | 784 | |
| UNII | BBX060AN9V | |
| KEGG | D00008 | |
| Propiedades físicas | ||
| Apariencia |
Incoloro | |
| Densidad | 1400 kg/m³; 1,4 g/cm³ | |
| Masa molar | 34,0147 g/mol | |
| Punto de fusión | 272,6 K (−1 °C) | |
| Punto de ebullición | 423,35 K (150 °C) | |
| Estructura cristalina | n/d | |
| Viscosidad | 1,245 cP a 20 °C | |
| Propiedades químicas | ||
| Acidez | 11,65 pKa | |
| Solubilidad en agua | Miscible | |
| Producto de solubilidad | n/d | |
| Momento dipolar | 2,26 D | |
| Termoquímica | ||
| ΔfH0gas | -136,11 kJ/mol | |
| ΔfH0líquido | -188 kJ/mol | |
| ΔfH0sólido | -200 kJ/mol | |
| S0gas, 1 bar | 232,95 J·mol–1·K | |
| S0líquido, 1 bar | 110 J·mol–1·K–1 | |
| Peligrosidad | ||
| SGA |
   | |
| NFPA 704 |
0
3
3
OX
| |
| Frases S | S1 S2 S17 S26 S28 S36 S37 S39 S45 | |
| Riesgos | ||
| Riesgos principales | ¡Atención! las siguientes son indicaciones para el peróxido de hidrógeno puro y soluciones concentradas. | |
| Ingestión | Serios daños, posiblemente fatal. | |
| Inhalación | Irritación severa, corrosivo, posiblemente fatal. | |
| Piel | Corrosivo. Agente aclarante y desinfectante. Causa ardor casi inmediatamente. | |
| Ojos | Altamente peligroso. Visión borrosa, quemaduras profundas graves | |
| Compuestos relacionados | ||
| Otros aniones | ? | |
| Otros cationes | Peróxido de sodio | |
| Compuestos relacionados | Agua, ozono, hidracina | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
A temperatura ambiente es un líquido incoloro de olor penetrante y desagradable. En el aire se encuentran de manera natural pequeñas cantidades de peróxido de hidrógeno gaseoso. El peróxido de hidrógeno es muy inestable. Se descompone lentamente en oxígeno y agua, con liberación de gran cantidad de calor. Su velocidad de descomposición puede aumentar mucho en presencia de catalizadores.
Aunque no es inflamable, es un agente oxidante potente que cuando entra en contacto con materia orgánica o algunos metales, como el cobre, la plata o el bronce puede causar combustión espontánea.
El peróxido de hidrógeno se encuentra en bajas concentraciones (3 a 9 %) en muchos productos domésticos para usos medicinales y como blanqueador de vestimenta y del cabello. En la industria se usa en concentraciones más altas, para blanquear telas y pasta de papel, y a 90 % como componente de combustibles para cohetes y para fabricar espuma de caucho y sustancias químicas orgánicas. En otras áreas, como en la investigación, se utiliza para medir la actividad de algunas enzimas, como la catalasa. Louis Jacques Thénard aisló el peróxido de hidrógeno (agua oxigenada) en 1818 a través de su trabajo con ácidos. Thénard observó que al tratar ácido bórico con ácido sulfúrico y luego destilar el producto resultante, se obtenía un líquido que mostraba propiedades interesantes. Este líquido, que más tarde se identificó como peróxido de hidrógeno, se caracterizó por su capacidad para liberar oxígeno y sus propiedades desinfectantes.
Thénard describió sus observaciones en su trabajo "Recherches sur la nature de l'acide boracique, et sur les combinaisons qu'il peut former" (Investigaciones sobre la naturaleza del ácido bórico y las combinaciones que puede formar). Su descubrimiento contribuyó significativamente al conocimiento de este compuesto, aunque en ese momento no se comprendían completamente todas sus propiedades y aplicaciones.
