| Thiophène |

|
| Structure chimique du thiophène |
| Identification |
| Nom UICPA
|
Thiophène
|
| Synonymes
|
Sulfure de divinylène
Thiacyclopentadiène
Thiofurane
|
| No CAS
|
110-02-1
|
| No ECHA
|
100.003.392 |
| No CE
|
203-729-4
|
| No RTECS
|
XM7350000
|
| PubChem
|
8030
|
| ChEBI
|
30856
|
| SMILES
|
|
| InChI
|
Std. InChI : vue 3D InChI =1S/C4H4S/c1-2-4-5-3-1/h1-4H Std. InChIKey : YTPLMLYBLZKORZ-UHFFFAOYSA-N |
| Apparence
|
liquide incolore, d'odeur âcre[1] rappelant celle du benzène[2].
|
| Propriétés chimiques |
| Formule
|
C4H4S [Isomères]
|
| Masse molaire[3]
|
84,14 ± 0,008 g/mol
C 57,1 %, H 4,79 %, S 38,11 %,
|
| pKa
|
38,4
|
| Moment dipolaire
|
0,55 ± 0,01 D [4]
|
| Propriétés physiques |
| T° fusion
|
−38 °C[1]
|
| T° ébullition
|
84 °C[1]
|
| Solubilité
|
dans l'eau : nulle[1]
|
| Paramètre de solubilité δ
|
20,1 MPa1/2 (25 °C)[5]
|
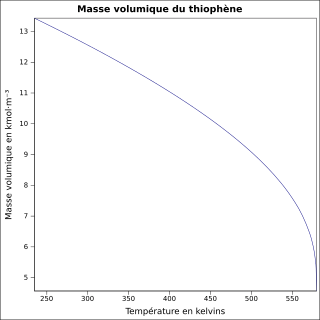
| Masse volumique
|
1,06 g·cm-3[1] à 20 °C,
2,9 (air = 1)
équation[6] : 
Masse volumique du liquide en kmol·m-3 et température en kelvins, de 234,94 à 579,35 K.
Valeurs calculées :
1,05869 g·cm-3 à 25 °C.
| T (K) |
T (°C) |
ρ (kmol·m-3) |
ρ (g·cm-3) |
|---|
| 234,94 |
−38,21 |
13,431 |
1,13011 |
| 257,9 |
−15,25 |
13,12966 |
1,10476 |
| 269,38 |
−3,77 |
12,97626 |
1,09185 |
| 280,86 |
7,71 |
12,82073 |
1,07876 |
| 292,34 |
19,19 |
12,66294 |
1,06549 |
| 303,82 |
30,67 |
12,50275 |
1,05201 |
| 315,3 |
42,15 |
12,33998 |
1,03831 |
| 326,78 |
53,63 |
12,17445 |
1,02438 |
| 338,26 |
65,11 |
12,00595 |
1,0102 |
| 349,74 |
76,59 |
11,83426 |
0,99576 |
| 361,22 |
88,07 |
11,6591 |
0,98102 |
| 372,7 |
99,55 |
11,48017 |
0,96596 |
| 384,18 |
111,03 |
11,29714 |
0,95056 |
| 395,66 |
122,51 |
11,10959 |
0,93478 |
| 407,15 |
134 |
10,91706 |
0,91858 |
|
| T (K) |
T (°C) |
ρ (kmol·m-3) |
ρ (g·cm-3) |
|---|
| 418,63 |
145,48 |
10,71901 |
0,90192 |
| 430,11 |
156,96 |
10,51477 |
0,88473 |
| 441,59 |
168,44 |
10,30357 |
0,86696 |
| 453,07 |
179,92 |
10,08442 |
0,84852 |
| 464,55 |
191,4 |
9,85614 |
0,82932 |
| 476,03 |
202,88 |
9,61719 |
0,80921 |
| 487,51 |
214,36 |
9,36559 |
0,78804 |
| 498,99 |
225,84 |
9,09865 |
0,76558 |
| 510,47 |
237,32 |
8,81266 |
0,74152 |
| 521,95 |
248,8 |
8,50217 |
0,71539 |
| 533,43 |
260,28 |
8,15861 |
0,68648 |
| 544,91 |
271,76 |
7,7672 |
0,65355 |
| 556,39 |
283,24 |
7,29805 |
0,61407 |
| 567,87 |
294,72 |
6,66952 |
0,56119 |
| 579,35 |
306,2 |
4,566 |
0,38419 |
|
|
| T° d'auto-inflammation
|
395 °C[1]
|
| Point d’éclair
|
−1 °C[1] ; −9 °C
|
| Limites d’explosivité dans l’air
|
1,5–12,5 %vol[1]
|
| Pression de vapeur saturante
|
à 12,5 °C : 5,3 kPa[1]
équation[6] : 
Pression en pascals et température en kelvins, de 234,94 à 579,35 K.
Valeurs calculées :
10 483,64 Pa à 25 °C.
| T (K) |
T (°C) |
P (Pa) |
|---|
| 234,94 |
−38,21 |
185,38 |
| 257,9 |
−15,25 |
1 058,43 |
| 269,38 |
−3,77 |
2 215,87 |
| 280,86 |
7,71 |
4 315,29 |
| 292,34 |
19,19 |
7 891,54 |
| 303,82 |
30,67 |
13 660,3 |
| 315,3 |
42,15 |
22 534,12 |
| 326,78 |
53,63 |
35 629,58 |
| 338,26 |
65,11 |
54 265,36 |
| 349,74 |
76,59 |
79 952,78 |
| 361,22 |
88,07 |
114 380,91 |
| 372,7 |
99,55 |
159 398,72 |
| 384,18 |
111,03 |
216 996,9 |
| 395,66 |
122,51 |
289 291,71 |
| 407,15 |
134 |
378 512,81 |
|
| T (K) |
T (°C) |
P (Pa) |
|---|
| 418,63 |
145,48 |
486 996,39 |
| 430,11 |
156,96 |
617 184,63 |
| 441,59 |
168,44 |
771 632,1 |
| 453,07 |
179,92 |
953 019,1 |
| 464,55 |
191,4 |
1 164 172,14 |
| 476,03 |
202,88 |
1 408 091,34 |
| 487,51 |
214,36 |
1 687 984,58 |
| 498,99 |
225,84 |
2 007 308,42 |
| 510,47 |
237,32 |
2 369 815,64 |
| 521,95 |
248,8 |
2 779 609,63 |
| 533,43 |
260,28 |
3 241 206 |
| 544,91 |
271,76 |
3 759 601,92 |
| 556,39 |
283,24 |
4 340 353,94 |
| 567,87 |
294,72 |
4 989 665,33 |
| 579,35 |
306,2 |
5 714 500
|
|
 |
| Thermochimie |
| S0liquide, 1 bar
|
181 J/mol·K
|
| ΔfH0gaz
|
115,0 kJ/mol
|
| ΔfH0liquide
|
81 kJ/mol
|
| Cp
|
122.4 J/mol·K (liq.)
équation[6] : 
Capacité thermique du liquide en J·kmol-1·K-1 et température en kelvins, de 234,94 à 357,31 K.
Valeurs calculées :
119,703 J·mol-1·K-1 à 25 °C.
T
(K) |
T
(°C) |
Cp
 |
Cp
 |
|---|
| 234,94 |
−38,21 |
111 630 |
1 327 |
| 243 |
−30,15 |
112 661 |
1 339 |
| 247 |
−26,15 |
113 173 |
1 345 |
| 251 |
−22,15 |
113 684 |
1 351 |
| 255 |
−18,15 |
114 195 |
1 357 |
| 259 |
−14,15 |
114 707 |
1 363 |
| 263 |
−10,15 |
115 218 |
1 369 |
| 267 |
−6,15 |
115 729 |
1 375 |
| 271 |
−2,15 |
116 239 |
1 381 |
| 275 |
1,85 |
116 750 |
1 388 |
| 279 |
5,85 |
117 261 |
1 394 |
| 283 |
9,85 |
117 771 |
1 400 |
| 287 |
13,85 |
118 281 |
1 406 |
| 292 |
18,85 |
118 919 |
1 413 |
| 296 |
22,85 |
119 429 |
1 419 |
|
T
(K) |
T
(°C) |
Cp
 |
Cp
 |
|---|
| 300 |
26,85 |
119 939 |
1 425 |
| 304 |
30,85 |
120 449 |
1 431 |
| 308 |
34,85 |
120 958 |
1 438 |
| 312 |
38,85 |
121 468 |
1 444 |
| 316 |
42,85 |
121 977 |
1 450 |
| 320 |
46,85 |
122 487 |
1 456 |
| 324 |
50,85 |
122 996 |
1 462 |
| 328 |
54,85 |
123 505 |
1 468 |
| 332 |
58,85 |
124 014 |
1 474 |
| 336 |
62,85 |
124 523 |
1 480 |
| 340 |
66,85 |
125 031 |
1 486 |
| 345 |
71,85 |
125 667 |
1 494 |
| 349 |
75,85 |
126 175 |
1 500 |
| 353 |
79,85 |
126 683 |
1 506 |
| 357,31 |
84,16 |
127 230 |
1 512 |
|

équation[7] : 
Capacité thermique du gaz en J·mol-1·K-1 et température en kelvins, de 50 à 1 500 K.
Valeurs calculées :
72,934 J·mol-1·K-1 à 25 °C.
T
(K) |
T
(°C) |
Cp
 |
Cp
 |
|---|
| 50 |
−223,15 |
28 848 |
343 |
| 146 |
−127,15 |
44 479 |
529 |
| 195 |
−78,15 |
53 342 |
634 |
| 243 |
−30,15 |
62 363 |
741 |
| 291 |
17,85 |
71 559 |
850 |
| 340 |
66,85 |
80 975 |
962 |
| 388 |
114,85 |
90 093 |
1 071 |
| 436 |
162,85 |
98 989 |
1 176 |
| 485 |
211,85 |
107 735 |
1 280 |
| 533 |
259,85 |
115 884 |
1 377 |
| 581 |
307,85 |
123 544 |
1 468 |
| 630 |
356,85 |
130 798 |
1 554 |
| 678 |
404,85 |
137 303 |
1 632 |
| 726 |
452,85 |
143 183 |
1 702 |
| 775 |
501,85 |
148 523 |
1 765 |
|
T
(K) |
T
(°C) |
Cp
 |
Cp
 |
|---|
| 823 |
549,85 |
153 103 |
1 820 |
| 871 |
597,85 |
157 050 |
1 866 |
| 920 |
646,85 |
160 455 |
1 907 |
| 968 |
694,85 |
163 220 |
1 940 |
| 1 016 |
742,85 |
165 476 |
1 967 |
| 1 065 |
791,85 |
167 326 |
1 989 |
| 1 113 |
839,85 |
168 780 |
2 006 |
| 1 161 |
887,85 |
169 977 |
2 020 |
| 1 210 |
936,85 |
171 052 |
2 033 |
| 1 258 |
984,85 |
172 090 |
2 045 |
| 1 306 |
1 032,85 |
173 254 |
2 059 |
| 1 355 |
1 081,85 |
174 735 |
2 077 |
| 1 403 |
1 129,85 |
176 645 |
2 099 |
| 1 451 |
1 177,85 |
179 194 |
2 130 |
| 1 500 |
1 226,85 |
182 663 |
2 171 |
|
|
| Propriétés électroniques |
| 1re énergie d'ionisation
|
8,86 ± 0,02 eV (gaz)[8]
|
| Propriétés optiques |
| Indice de réfraction
|
1,529 (20 °C)
|
| Précautions |
| SGH[2] |
  Danger H225 : Liquide et vapeurs très inflammables
H302 : Nocif en cas d'ingestion
H319 : Provoque une sévère irritation des yeux
H412 : Nocif pour les organismes aquatiques, entraîne des effets à long terme
P210 : Tenir à l’écart de la chaleur/des étincelles/des flammes nues/des surfaces chaudes. — Ne pas fumer.
P260 : Ne pas respirer les poussières/fumées/gaz/brouillards/vapeurs/aérosols.
P262 : Éviter tout contact avec les yeux, la peau ou les vêtements.
P273 : Éviter le rejet dans l’environnement.
P305+P351+P338 : En cas de contact avec les yeux : rincer avec précaution à l’eau pendant plusieurs minutes. Enlever les lentilles de contact si la victime en porte et si elles peuvent être facilement enlevées. Continuer à rincer.
P403+P235 : Stocker dans un endroit bien ventilé. Tenir au frais.
|
| NFPA 704 |
|
| Transport[2] |
Code Kemler :33 : matière liquide très inflammable (point d'éclair inférieur à 23 °C) Numéro ONU :2414 : THIOPHÈNE Classe :3 Étiquette : 3 3 : Liquides inflammables Emballage :Groupe d'emballage II : matières moyennement dangereuses ; |
| Écotoxicologie |
| LogP
|
1,81[1]
|
|
| Unités du SI et CNTP, sauf indication contraire. |
modifier  |













