
Trisilane
composé chimique / De Wikipedia, l'encyclopédie encyclopedia
Le trisilane est un composé chimique de formule Si3H8. Ce silane est l'analogue structurel silicié du propane C3H8. Il se présente sous la forme d'un liquide incolore pyrophorique ayant une pression de vapeur élevée, d'où un risque explosif important[1].
| Trisilane | |
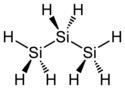 | |
| Structure du trisilane | |
| Identification | |
|---|---|
| No CAS | 7783-26-8 |
| No ECHA | 100.132.113 |
| No CE | 616-514-9 |
| PubChem | 139070 |
| SMILES | |
| InChI | |
| Apparence | liquide incolore[1] |
| Propriétés chimiques | |
| Formule | H8Si3 [Isomères]Si3H8 |
| Masse molaire[2] | 92,32 ± 0,001 5 g/mol H 8,73 %, Si 91,27 %, |
| Propriétés physiques | |
| T° fusion | −114,8 °C[1] |
| T° ébullition | 52,8 °C[1] |
| Masse volumique | 0,739 g·cm-3[1] |
| Précautions | |
| SGH[3] | |
| H224, H250, H261, H315, H319 et H335 H224 : Liquide et vapeurs extrêmement inflammables H250 : S'enflamme spontanément au contact de l'air H261 : Dégage, au contact de l'eau, des gaz inflammables H315 : Provoque une irritation cutanée H319 : Provoque une sévère irritation des yeux H335 : Peut irriter les voies respiratoires |
|
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le trisilane a été obtenu pour la première fois par Alfred Stock en faisant réagir de l'acide chlorhydrique HCl sur du siliciure de magnésium Mg2Si[4],[5]. Cette réaction a par la suite été exploitée par Friedrich Wöhler et Heinrich Buff, puis approfondie par Henri Moissan et Samuel Smiles en 1902[6].
Le trisilane peut également être obtenu en faisant réagir de l'octachlorotrisilane Si3Cl8 avec de l'aluminohydrure de lithium LiAlH4 ou par pyrolyse du disilane Si2H6[1] :
Comme les autres silanes, il peut également être isolé par distillation fractionnée du mélange de silanes obtenu par décomposition acide du siliciure de magnésium ou par décharges électrostatiques sur du silane SiH4[1].
La principale propriété du trisilane est son instabilité thermique. Il se décompose en laissant un dépôt de silicium et en libérant du silane selon l'équation idéalisée[7] :
Le trisilane a été étudié dans le cadre de l'application de couches minces de silicium dans l'industrie des semiconducteurs. La thermolyse du trisilane permet d'obtenir des nanofils de silicium[8].

