
Ibridizzazione
combinazione di un certo numero di orbitali / Da Wikipedia, l'enciclopedia encyclopedia
Caro Wikiwand AI, Facciamo breve rispondendo semplicemente a queste domande chiave:
Puoi elencare i principali fatti e statistiche su Ibridizzazione?
Riassumi questo articolo per un bambino di 10 anni
L'ibridazione (o ibridizzazione[1]) è un procedimento di combinazione matematica di un certo numero di orbitali atomici (orbitali s, p, d) di valenza di un atomo, aventi energie poco diverse, che permette di ottenere per quell'atomo altrettanti nuovi orbitali ibridi equivalenti (isoenergetici tra loro, finché possibile), coi lobi orientati lungo le direzioni dettate dalla combinazione matematica stessa. Questi nuovi orbitali ibridi potranno essere usati dall'atomo per formare legami con altri atomi. Verrà preferito l'uso di orbitali ibridi, rispetto a quello di orbitali atomici, se i legami con essi formati con altri atomi comporterà un guadagno di stabilità per la molecola (legami più forti).
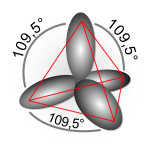
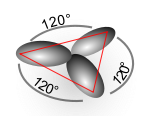
Il numero di orbitali ibridi ottenuti è uguale al numero di quelli che vengono combinati, cosicché il numero totale di orbitali di valenza dell'atomo non cambia. I lobi degli orbitali ibridi hanno nuove direzioni rispetto a quelli atomici e tali direzioni formano tra loro angoli caratteristici per ogni combinazione (sp, sp2, sp3...).
Il processo di ibridazione può essere accompagnato da un processo di promozione di uno o più elettroni in orbitali a livello energetico più alto allo scopo di ottenere un maggior numero di elettroni spaiati; questo ha ovviamente un costo energetico che però può spesso (non sempre) essere più che compensato dal guadagno connesso con la formazione di un numero maggiore di legami e, come accennato sopra, legami più forti.
L'ibridazione consente di stabilire la forma geometrica di una molecola o di uno ione con il metodo di Gillespie (1957), che è un affinamento della teoria già elaborata nel 1940 da Nevil Sidgwick e Herbert Marcus Powell.
Le ibridazioni degli orbitali s e p possono essere di tipo:
- sp (dà luogo a due orbitali ibridi e strutture lineari);[2] esempi di ibridazione sp si hanno nelle molecole di azoto (N2), monossido di carbonio (CO), acetilene (C2H2), e fluoruro di berillio (BeF2);
- sp2 (dà luogo a tre orbitali ibridi e strutture trigonali planari);[3] esempi di ibridazione sp2 si hanno nelle molecole di trifluoruro di boro (BF3), triossido di zolfo (SO3), diossido di zolfo (SO2), etene (C2H4), benzene (C6H6) e grafene;
- sp3 (dà luogo a quattro orbitali ibridi e strutture tetraedriche).[4] esempi di ibridazione sp3 si hanno nelle molecole di metano (CH4), ammoniaca (NH3), acqua (H2O), acido perclorico (HClO4), acido solforico (H2SO4) e acido fosforico (H3PO4).
Si possono avere inoltre altri tipi di ibridazione: sp3d, sp3d2, ed altre ancora.[5]