
Natrium bikarbonat
From Wikipedia, the free encyclopedia
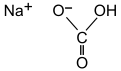
Natrium bikarbonat atau soda penaik ialah sebatian kimia natrium dengan formula kimia NaHCO3.
Fakta Segera Nama, Pengecam ...
 | |||
| |||
 | |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC
Natrium hidrogen karbonat Sodium hydrogen carbonate | |||
| Nama lain
Soda penaik | |||
| Pengecam | |||
| |||
Imej model 3D Jmol |
|||
| 4153970 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider |
| ||
| DrugBank |
| ||
| ECHA InfoCard | 100.005.122 | ||
| Nombor EC |
| ||
| Nombor E | E500(ii) (pengawal keasidan pH & agen antikerakan) | ||
| KEGG |
| ||
| MeSH | Sodium+bicarbonate | ||
PubChem CID |
|||
| Nombor RTECS |
| ||
| UNII | |||
CompTox Dashboard (EPA) |
|||
| |||
| |||
| Sifat | |||
| NaHCO3 | |||
| Jisim molar | 84.0066 g mol−1 | ||
| Rupa bentuk | Hablur putih | ||
| Bau | Tidak berbau | ||
| Ketumpatan |
| ||
| Takat lebur | (Terurai menjadi natrium karbonat dari suhu 50 °C[1][2]) | ||
| Keterlarutan | 0.02 wt% aseton, 2.13 wt% metanol pada 22 °C.[5] tidak larut dalam etanol | ||
| log P | −0.82 | ||
| Keasidan (pKa) | |||
Indeks biasan (nD) |
nα = 1.377 nβ = 1.501 nγ = 1.583 | ||
| Struktur | |||
| Struktur kristal | Monoklin | ||
| Termokimia | |||
| Muatan haba tentu, C | 87.6 J/mol K[7] | ||
| Entropi molar piawai S |
101.7 J/mol K[7] | ||
Entalpi pembentukan piawai (ΔfH⦵298) |
−950.8 kJ/mol[7] | ||
Tenaga bebas Gibbs (ΔfG˚) |
−851.0 kJ/mol[7] | ||
| Farmakologi | |||
| Kod ATC | B05CB04 B05XA02, QG04BQ01 (WHO) | ||
| Kaedah pemberian | IV, oral | ||
| Bahaya | |||
| Bahaya-bahaya utama | Menyebabkan kegatalan mata teruk | ||
| MSDS | External MSDS | ||
| NFPA 704 (berlian api) | |||
| Takat kilat | Incombustible | ||
| Dos maut (LD) atau kepekatan dos maut (LC) | |||
LD50 (median dos) |
4220 mg/kg (tikus, oral)[8] | ||
| Sebatian berkaitan | |||
Anion lain |
Natrium karbonat | ||
Kation lain |
| ||
Sebatian berkaitan |
| ||
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |||
| | |||
| Rujukan kotak info | |||
Tutup


