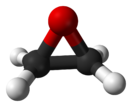
Окись этилена
химическое соединение / Материал из Википедии — свободной encyclopedia
Уважаемый Wikiwand AI, давайте упростим задачу, просто ответив на эти ключевые вопросы:
Перечислите основные факты и статистические данные о Окись этилена?
Кратко изложите эту статью для 10-летнего ребёнка
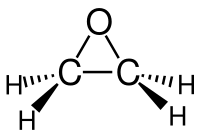
Оксира́н (этиленокси́д, о́кись этиле́на, 1,2-эпоксиэтáн) — органическое химическое гетероциклическое вещество, химическая формула C2H4O. При нормальных условиях — бесцветный газ с характерным сладковатым запахом. Производное этилена и представляет собой простейший эпоксид — трёхчленный гетероцикл, в кольцевой молекуле которого содержатся один атом кислорода и два атома углерода.
| Окись этилена | |||
|---|---|---|---|
  | |||
| Общие | |||
| Систематическое наименование |
оксиран | ||
| Традиционные названия | этиленоксид, 1,2-эпоксиэтан, этилена окись | ||
| Хим. формула | C2H4O | ||
| Рац. формула | C2H4O | ||
| Физические свойства | |||
| Состояние | газ | ||
| Молярная масса | 44,0526 г/моль | ||
| Плотность | (относительно воды[прояснить] при температуре 10 °C для жидкой окиси этилена)[1] 0,8824 г/см³ | ||
| Энергия ионизации | 10,56 ± 0,01 эВ[2] и 10,57 эВ[3] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | −111,3[4] | ||
| • кипения | 10,7[5] °C | ||
| • вспышки | < −18[5] °C | ||
| Пределы взрываемости | 3 ± 1 об.%[2] | ||
| Критическая точка | 195,8 °C; 7,19 МПа[5] | ||
| Мол. теплоёмк. | 48,19[6] Дж/(моль·К) | ||
| Энтальпия | |||
| • образования | −51,04[6] кДж/моль | ||
| Удельная теплота испарения | 25,82[5] | ||
| Удельная теплота плавления | 5,17[5] | ||
| Давление пара | 145,8 кПа (при 20 °C)[5] | ||
| Оптические свойства | |||
| Показатель преломления | 1,35965 (при 7 °C)[6] | ||
| Структура | |||
| Дипольный момент | 6,3E−30 Кл·м[3] | ||
| Классификация | |||
| Рег. номер CAS | 75-21-8 | ||
| PubChem | 6354 | ||
| Рег. номер EINECS | 200-849-9 | ||
| SMILES | |||
| InChI | |||
| RTECS | KX2450000 | ||
| ChEBI | 27561 | ||
| ChemSpider | 6114 | ||
| Безопасность | |||
| Предельная концентрация | 1 мг/м³ | ||
| ЛД50 | 72 мг/кг | ||
| Токсичность | высокая | ||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Благодаря особенностям электронной структуры молекулы, окись этилена легко вступает в реакции присоединения с раскрытием гетероцикла и поэтому легко подвергается полимеризации.
Смесь паров вещества с воздухом является чрезвычайно огне- и взрывоопасной.
Окись этилена обладает дезинфицирующими свойствами, то есть, является сильным ядом для большинства известных микроорганизмов даже в газообразном виде, что используется для газовой стерилизации, например, одноразовых медицинских шприцев.
Также является медленно действующим сильным ядом для теплокровных животных и человека, проявляя канцерогенное, мутагенное, раздражающее и наркотическое действие.
Окись этилена является одним из важных веществ в основном органическом синтезе и широко используется для получения многих химических веществ и полупродуктов, в частности этиленгликолей, этаноламинов, простых и сложных гликолевых и полигликолевых эфиров и прочих соединений.
В химической промышленности окись этилена получают прямым окислением этилена в присутствии серебряного катализатора.