
Плутоний
химический элемент / Материал из Википедии — свободной encyclopedia
Уважаемый Wikiwand AI, давайте упростим задачу, просто ответив на эти ключевые вопросы:
Перечислите основные факты и статистические данные о Плутоний?
Кратко изложите эту статью для 10-летнего ребёнка
Плуто́ний (обозначается символом Pu; атомное число 94) — тяжёлый хрупкий высокотоксичный радиоактивный металл серебристо-белого цвета[10][11]. В периодической таблице располагается в семействе актиноидов.
| Плутоний | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ← Нептуний | Америций → | |||||||||||||||
| |||||||||||||||
| Внешний вид простого вещества | |||||||||||||||
| Радиоактивный серебристый металл | |||||||||||||||
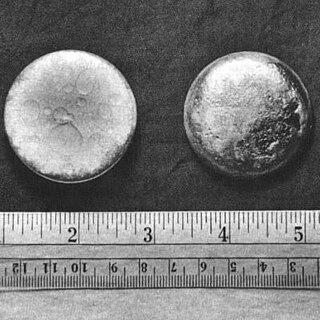 Образец плутония |
|||||||||||||||
| Свойства атома | |||||||||||||||
| Название, символ, номер | Плуто́ний / Plutonium (Pu), 94 | ||||||||||||||
| Тип группы | Актиноиды | ||||||||||||||
| Группа, период, блок | 7, 3, f | ||||||||||||||
| Атомная масса (молярная масса) |
244,0642 а. е. м. (г/моль) | ||||||||||||||
| Электронная конфигурация | [Rn] 5f6 7s2 | ||||||||||||||
| Радиус атома | 162[1][2] пм | ||||||||||||||
| Химические свойства | |||||||||||||||
| Радиус Ван-дер-Ваальса | 200[3] пм | ||||||||||||||
| Радиус иона |
Pu3+: 100 пм, Pu4+: 86 пм, Pu5+: 74 пм, Pu6+: 71[4] пм |
||||||||||||||
| Электроотрицательность | 1,28 (шкала Полинга) | ||||||||||||||
| Электродный потенциал |
Pu←Pu4+ −1,25 В, Pu←Pu3+ −2,0 В, Pu←Pu2+ −1,2 В |
||||||||||||||
| Степени окисления | +2, +3, +4, +5, +6, +7[5] | ||||||||||||||
| Энергия ионизации (первый электрон) |
584,7 (6,06)[6] кДж/моль (эВ) | ||||||||||||||
| Термодинамические свойства простого вещества | |||||||||||||||
| Термодинамическая фаза | Металл | ||||||||||||||
| Плотность (при н. у.) | 19,84 г/см³ | ||||||||||||||
| Температура плавления | 639,7 °C; 912 K; 1182 °F [1] | ||||||||||||||
| Температура кипения | 3235 °C; 3507 K; 5855 °F [1] | ||||||||||||||
| Мол. теплота плавления | 2,8 кДж/моль | ||||||||||||||
| Мол. теплота испарения | 343,5 кДж/моль | ||||||||||||||
| Молярная теплоёмкость | 32,77[7] Дж/(K·моль) | ||||||||||||||
| Молярный объём | 12,12 см³/моль | ||||||||||||||
|
|||||||||||||||
| Кристаллическая решётка простого вещества | |||||||||||||||
| Структура решётки | Моноклинная | ||||||||||||||
| Параметры решётки |
a=6,183 Å b=4,822 Å c=10,963 Å β=101,8°[9] |
||||||||||||||
| Температура Дебая | 162 K | ||||||||||||||
| Прочие характеристики | |||||||||||||||
| Теплопроводность | (300 K) 6,74 Вт/(м·К) | ||||||||||||||
| Скорость звука | 2260[6] м/с | ||||||||||||||
| Номер CAS | 7440-07-5 | ||||||||||||||
| 94 | Плутоний |
(244) | |
| 5f67s2 | |
Для этого элемента характерны существенно отличающиеся от остальных элементов структурные и физико-химические свойства[10]. Плутоний имеет семь аллотропных модификаций при определённых температурах и диапазонах давления[12]: α, β, γ, δ, δ', ε и ζ. Может принимать степени окисления от +2 до +7, основными считаются +4, +5, +6. Плотность варьируется от 19,8 (α-Pu) до 15,9 г/см³ (δ-Pu).
Плутоний не имеет стабильных изотопов[5]. В природе в следовых количествах присутствуют самый долгоживущий изотоп из всех трансурановых элементов 244Pu и его дочерний нуклид 240Pu, а также 239Pu[1][13][14] и 238Pu. В окружающей среде находится преимущественно в виде диоксида (PuO2), который в воде менее растворим, чем песок (кварц)[11]. Нахождение элемента в природе настолько мало, что его добыча нецелесообразна[~ 1].
Второй после нептуния (который был ошибочно «получен» в 1934 году группой Энрико Ферми[15][16]; его первый изотоп 239Np синтезирован и идентифицирован в мае 1940 года Эдвином Макмилланом и Филипом Абельсоном[17][18][19]) искусственный элемент, полученный в чрезвычайно маленьких количествах в конце 1940 г. в виде изотопа 238Pu[13].
Первый искусственный химический элемент, производство которого началось в промышленных масштабах[20] (в СССР с 1946 года в Челябинске-40 было создано предприятие по производству оружейного урана и плутония[21]). США, а затем и СССР были первыми странами, освоившими его получение.
Плутоний получают из природного изотопа урана U238. Общее количество плутония, хранящегося в мире во всевозможных формах, оценивалось в 2003 г. в 1239 т[22].
Плутоний используется в производстве ядерного оружия (так называемый «оружейный плутоний»), топлива для ядерных реакторов гражданского и исследовательского назначения и в качестве источника энергии для космических аппаратов[23]. В первой ядерной бомбе в мире, созданной и испытанной в 1945 году в США, использовался плутониевый заряд. Того же типа была и первая атомная бомба, испытанная СССР в 1949 году[24].
В таблице справа приведены основные свойства для α-плутония. Данная аллотропная модификация является основной для плутония при комнатной температуре и нормальном давлении.
- 7440-07-5 для плутония неспецифического состава,
- 13981-16-3 для 238Pu,
- 15117-48-3 для 239Pu,
- 14119-33-6 для 240Pu.
