Астат (ад грэц. astatos — «няўстойлівы», па-лацінску: Astatium) At — хімічны элемэнт 17 (VIIa) групы пэрыядычнай сыстэмы; атамны нумар 85. Самы цяжкі галяген. Вядомы 31 ізатоп астату з масавымі нумарамі ад 193 да 223 і яны ўсе радыяактыўныя. Утрыманьне ў прыродзе крайне нязначнае. Самы рэдкі элемэнт, які сустракаецца на Зямлі. Ён увесь час утвараецца ў паверхневым пласце Зямной кары, але хутка распадаецца. Назіраюцца ізатопы 218At ад радыяактыўнага шэрагу распаду ўрана, 216At ад радыяактыўнага шэрагу тору, 215At і 219At ад радыяактыўнага шэрагу актыну. Паводле ацэнак, у кожны момант існуе менш за 30 мг At. Упершыню атрыманы у 1940 годзе. Дэйлам Корсанам (Dale R. Corson), Кэнэтам МакКэнзі (Kenneth R. MacKenzie), Эміліё Сэгрэ ва Унівэрсытэце Каліфорніі (ЗША). Яны апраменьвалі 209Bi альфа-часьцінкамі ад цыклятрона. У выніку атрымліваўся ізатоп 211At і два нэўтрона. Акрамя названага мэтаду атрыманьня астат таксама атрымліваюць апрамяненьнем тору альфа-часціцамі высокіх энэргій. У лябараторных умовах удаецца атрымаць усяго каля 0,001 мкг астату. Пры гэтым яго прыходзіцца ахаладжаць, бо з-за хуткага радыяактыўнага распаду ён награваецца і выпарваецца. Агулам дагэтуль штучна атрымана ўсяго каля 0,05 мкг астату і фактычна ўвесь ён ужо распаўся. З-за таго, што астат так цяжка атрымаць у вялікай колькасьці, на сёньняшні дзень ён не выкарыстоўваецца нідзе акрамя фундамэнтальных навуковых дасьледаваньняў. З-за высокай радыёактыўнасьці астат вымагае сур'ёзных захадаў бясьпекі. Па хімічных уласьцівасцях падобны да немэталу ёду. У прыватнасьці, лічыцца, што ўнутры арганізма вышэйшых жывёлаў астат гэтаксама як і ёд будзе назапашвацца ў шчытападобнай залозе. Паводле шэрагу іншых хімічных уласьцівасьцяў астат падобны да мэталаў палёну і бісмуту.
Quick Facts Выгляд, Агульная інфармацыя ...
|
|
| Выгляд |
 |
| Агульная інфармацыя |
| Назва, сымбаль, атамны нумар |
Астат, At, 85 |
| Катэгорыя элемэнту |
Паўмэталы |
| Група, пэрыяд, блёк |
17, 6, p |
| Адносная атамная маса |
(210) г·моль−1 |
| Канфігурацыя электронаў |
[Xe] 4f14 5d10 6s2 6p5 |
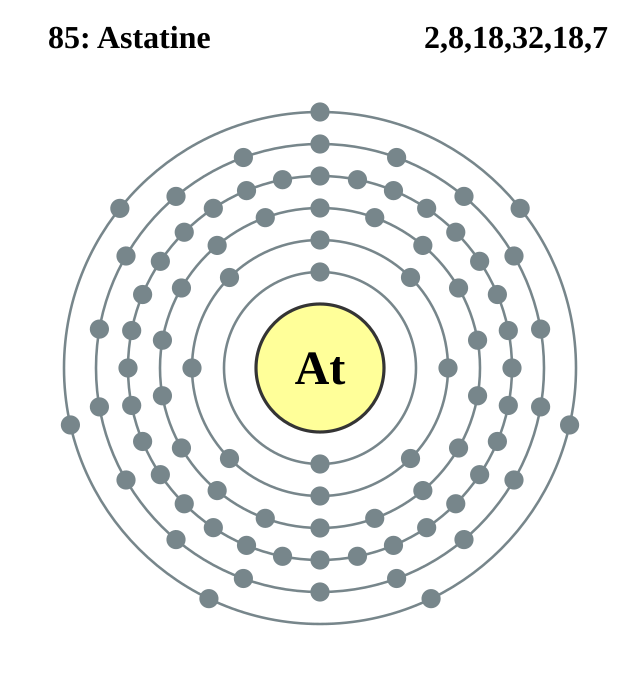
| Электронаў у абалонцы |
2, 8, 18, 32, 18, 7
 |
| Фізычныя ўласьцівасьці |
| Колер |
срэбны |
| Фаза |
цьвёрдае цела |
| Шчыльнасьць (пры п. т.) |
(ацэнка) 6,4 г·см−3 |
| Тэмпэратура плаўленьня |
575 K, 302 °C, 576 °F |
| Тэмпэратура кіпеньня |
(ацэнка) 337 °C |
| Удзельная цеплыня плаўленьня |
6 кДж·моль−1 |
| Удзельная цеплыня выпарваньня |
40 кДж·моль−1 |
| Цеплаправоднасьць |
(300 K) (ацэнка) 1,7 Вт·м−1·K−1 |
| Уласьцівасьці атама |
| Ступені затляненьня |
−1, +1, +3(?), +5, +7(?) |
| Электраадмоўнасьць |
2,2 |
| Энэргіі іянізацыі |
1-я: 920 кДж·моль−1 |
| Атамны радыюс (разл.) |
127 пм |
| Кавалентны радыюс |
150 пм |
| Іншыя характарыстыкі |
| Нумар CAS |
7440-68-8 |
| Найбольш стабільныя ізатопы |
| Асн. артыкул: ізатопы астату |
| іза |
% |
пэрыяд паўраспаду |
распад |
энэргія (МэВ) |
прадукты распаду |
|---|
| 210At |
- |
8,1 гадзін |
Эл. з. (99,82%) |
? |
210Po |
| α (0,18%) |
5,52 |
206Bi |
| 211At |
- |
7,214 гадзін |
Эл. з. (58,20%) |
? |
211Po |
| α (41,80%) |
5,87 |
207Bi |
|
|
Close


