
라이신
화합물 / From Wikipedia, the free encyclopedia
리신(영어: lysine) (기호: Lys or K)[2]은 단백질의 생합성에 사용되는 α-아미노산이다. 리신은 α-아미노기(생물학적 조건에서 양성자화된 −NH3+ 형태), α-카복실기(생물학적 조건에서 탈양성자화된 −COO− 형태) 및 곁사슬인 리실기((CH2)4NH2)를 포함하고 있다. 리신은 염기성 양전하(생리학적 pH에서), 지방족 아미노산으로 분류된다. 리신은 AAA, AAG 코돈에 의해 암호화되어 있다. 거의 모든 다른 아미노산들과 마찬가지로 α-탄소는 카이랄성이며, 리신은 2가지 거울상 이성질체 또는 2가지를 모두 포함하는 라세미 혼합물을 나타낼 수 있다. 이 문서에서 리신은 생물학적으로 활성인 거울상 이성질체인 L-리신을 의미하며, 여기서 α-탄소는 S 입체배치이다.
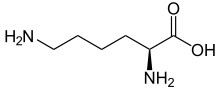 L-리신의 골격 구조식 | |||
| |||
| 이름 | |||
|---|---|---|---|
| IUPAC 이름
L-lysine
D-lysine | |||
| 체계명
(2S)-2,6-diaminohexanoic acid (L-lysine)
(2R)-2,6-diaminohexanoic acid (D-lysine) | |||
| 별칭
lysine, D-lysine, L-lysine, LYS, h-Lys-OH | |||
| 식별자 | |||
3D 모델 (JSmol) |
| ||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.000.673 | ||
| KEGG |
| ||
PubChem CID |
|||
| UNII |
| ||
CompTox Dashboard (EPA) |
|||
| |||
| |||
| 성질 | |||
| C6H14N2O2 | |||
| 몰 질량 | 146.190 g·mol−1 | ||
| 1.5 kg/L | |||
| 약리학 | |||
| B05XB03 (WHO) | |||
인체는 리신을 합성할 수 없다. 리신은 사람에서 필수 아미노산이며, 따라서 식사를 통해 섭취해야 한다. 리신을 합성하는 생물에서는 두 가지 주요 생합성 경로인 다이아미노피멜산 경로 및 α-아미노아디프산 경로가 존재하며, 이들 경로는 별개의 효소와 기질을 사용하고 다양한 생물에서 발견된다. 리신의 이화작용은 여러 대사 경로들 중 하나를 통해 일어나며, 이 중 가장 일반적인 경로는 사카로핀 경로이다.
리신은 사람에서 여러 역할들, 가장 중요하게는 단백질 생성 뿐만 아니라 콜라겐 폴리펩타이드의 가교 형성, 필수 미네랄 영양소의 흡수, 지방산 대사의 핵심적인 화합물인 카르니틴의 생성에서도 역할을 한다. 리신은 또한 종종 히스톤 변형에 관여하기 때문에 후성유전체에 영향을 미친다. ε-아미노기는 종종 수소 결합에 참여하고 촉매 작용의 일반 염기로 사용된다. ε-아미노기는 카복실기와 결합하고 있는 α-탄소로부터 4번째 탄소에 부착된다.[3]
여러 생물학적 과정에서 리신의 중요성으로 인해 리신이 부족하면 결합 조직의 결함, 지방산 대사의 장애, 빈혈 및 전신 단백질 에너지 결핍을 비롯한 여러 질병 상태가 발생할 수 있다. 대조적으로 비효율적인 이화작용으로 인한 과도한 리신은 심각한 신경 질환을 유발할 수 있다.
리신은 1889년에 독일의 생화학자 페르디난트 하인리히 에드문트 드레흐셀(Ferdinand Heinrich Edmund Drechsel)에 의해 우유의 카제인 단백질에서 처음으로 분리되었다.[4] 그는 분리한 물질을 "lysin"이라고 명명했다.[5] 1902년에 독일의 화학자 에밀 피셔와 프리츠 바이게르트(Fritz Weigert)는 합성을 통해 리신의 화학 구조를 결정했다.[6]

